
專屬客服號

微信訂閱號
全面提升數據價值
賦能業務提質增效
摘要:改善鋰離子電池正極材料的綜合性能一直是鋰離子電池研究中極為關鍵的部分。本文主要講述了鋰離子電池層狀正極材料的發展,從結構以及機理上介紹了不同層狀正極材料,并對各材料的優缺點進行了闡述。
鋰離子電池的突破性發展始于1980年,Armand等人首次提出了“搖椅式電池的概念:在充放電過程中,鋰離子在正極和負極之間來回嵌入和脫出,如此循環往復,以形成充放電的循環”。其中正極材料的成本大約占商業化鋰離子電池成本的40%,同時作為鋰的主要來源,所以正極材料的選擇與研究就顯得尤為重要。
鋰離子電池的正極材料一般選擇電勢相對較高且結構穩定的嵌鋰化合物,主要有層狀結構LiMO2(M=Ni、Co、Mn)、尖晶石結構LiM2O4和橄欖石結構LiFeO4。
傳統LiCoO2正極材料
1981年Goodenough等人首次提出了將層狀LiCoO2材料應用于鋰離子電池正極材料,隨后1991年SONY公司首次將其應用于商業化。LiCoO2具有典型的層狀結構,如圖所示,氧在結構中進行立方密堆積作為整體的結構框架,Li+離子和Co3+離子交替占據氧所形成的八面體空隙中。從宏觀上來看,這種所謂的層狀結構就是由一層氧、一層Li+離子、一層氧、一層Co3+離子、一層氧……如此循環堆積而成。在充電時,Li+離子在Li層的二維平面內擴散脫出進入電解液到達負極,放電時,Li+離子從負極進入電解液進而回到正極材料中Li層原本的位置,如此循環往復。但在高電壓充電下,LiCoO2中鋰離子的脫出量超過50%時,層狀宿主結構會發生結構變化甚至坍塌,進而使得電池失效,同時鈷資源較少、成本較高并且有一定的毒性,所以LiCoO2并不適合作為動力性鋰離子電池使用。
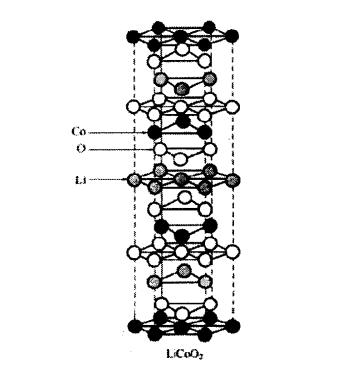
圖1
三元正極材料
與層狀LiCoO2材料結構類似的LiNiO2和LiMnO2材料中,LiNiO2具有倍率性能好、環境污染小、成本相對較低等特點,但同時也存在循環壽命短、熱穩定性差安全性不好等問題;而LiMnO2材料的結構穩定較差。三種層狀材料各有優點和缺點,為了達到更好的應用與資源利用,1999年三元層狀材料LiNixCoyMn1-x-yO2便由此被提出,利用三種LiCoO2 LiNiO2 LiMnO2材料的優點避其缺點。如圖2所示,從結構上來看,三元層狀材料可以看作是在LiCoO2的基礎上,在其Co元素層,用元素Ni和Mn對Co元素進行了部分替代,由于Ni、Co、Mn三種元素都處于元素周期表的第四周期,故可以形成這種LiNixCoyMn1-x-yO2所謂固溶體。由于Ni、Co和Mn三元的協同效應,使得三元材料具有良好的循環穩定性、倍率性能和熱穩定性。如在2001年由Ohzuku等人首次發表的關于1∶1∶1型LiNi1/3Co1/3Mn1/3O2材料,其中Ni、Co、Mn的化合價分別為+2、+3和+4價,Mn4+離子不具備電化學活性,但是能夠穩定材料結構,Co3+離子能夠抑制Ni2+離子與鋰層的Li+發生離子混排,同時提供參與電化學反應中提供容量,Ni2+離子參與電化學反應,作為主要的容量提供來源。在充放電循環過程中,Ni在+2~+4之間變化,Co則在+3~+4之間變化。雖然這種層狀三元LiNi1/3Co1/3Mn1/3O2材料具有較好的循環穩定性,但隨著研究發展,其容量已漸漸跟不上需求。目前提高Ni含量的三元層狀LiNi0.5Co0.2Mn0.3O2、LiNi0.6Co0.2Mn0.2O2和LiNi0.8Co0.1Mn0.1O2或是更高Ni含量的材料也在進一步的開發研究中。隨著Ni含量的升高,電池的容量也在逐步提高,但是也帶來了循環穩定性和熱穩定差等諸多問題,這些都問題有待科研工作者去進一步解決,以期得到三元層狀材料更好的商業化應用。
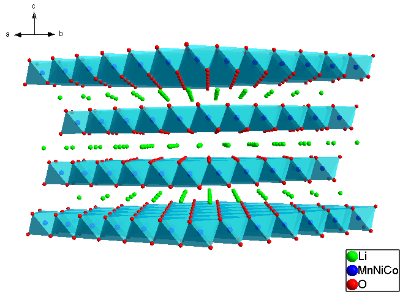
圖2
富鋰錳基正極材料
相比三元材料,富鋰錳基材料由于以Mn元素作為主要過渡金屬元素,其成本相對較低,對環境友好,最為重要的是,其具有三元材料所達不到的高比容量(>250mAh/g),是極有潛力的下一代鋰離子電池用正極材料。富鋰錳基材料可以寫成Li1+(x/(2+x))M1-(x/(2+x))O2(M=Ni、Co、Mn,0<x<1),亦可寫作xLi2MnO3·(1-x)LiMO2(M=Ni、Co、Mn,0<x<1)。自從富鋰錳基材料誕生以來,其結構便存在諸多爭議,近來,通過不同先進的物理表征方法,越來越多的研究者認同其具有兩相結構的觀點:即在xLi2MnO3·(1-x)LiMO2材料中包含兩種組分Li2MnO3和LiMO2。其中LiMO2即傳統的層狀三元結構;但li2mno3的結構有所特殊,正是由于這種結構特殊造成了富鋰錳基正極材料與傳統三元材料的各項不同。如圖3中Li2MnO3的結構可以看成是在傳統層狀limno2的基礎上,將其Mn層內的1/3Mn用Li進行取代,即鋰層和鋰/ 錳混合層交替排列,故而Li2MnO3的化學式也可以協作Li(Li1/3Mn2/3)O2,在鋰、錳混合層中,Li+離子和Mn4+離子以1∶2的比例交替有序排列,從c方向看即形成了limn6的花瓣狀分布,而在傳統三元層狀材料的過渡金屬層中,過渡金屬Ni、Co、Mn的分布是隨機的。更多鋰的存在使得富鋰錳基材料具有更為高的理論比容量。
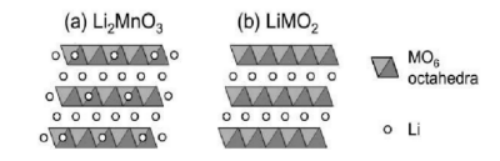
圖3
由于結構的不同,富鋰錳基材料和傳統三元材料在充放電機理上有所變化。第一次充電時,需要對Li2MnO3結構進行活化,充電電壓達到4.5V之前隨著Li+的脫出,發生Ni2+/Ni4+、Co3+/Co4+之間的氧化還原反應;當充電電壓到達4.5V時,Li2MnO3結構被活化,由于此結構中的Mn本已達到最高氧化態+4,所以在Li+脫出的同時由O2-參與氧化還原反應,根據近來研究者們所得出的結論,此過程由O2-失去電子成為O-或Ox-,這些被還原的O離子部分能夠穩定在結構中參與后續的反應,但部分會以O2或者CO2的形式析出材料結構,進而造成結構的永久不可逆轉變以及容量的不可逆損失。
雖然富鋰錳基材料具有較高的理論比容量,但正是由于這種特殊的氧化還原反應機制也造成了其結構的不穩定性,O離子參與氧化還原造成了后續的諸多問題:氧的流失直接導致了部分結構的塌縮,同時造成了其他過渡金屬元素Ni、Co、Mn的變化,這些過渡金屬元素會降低價態,并且過渡金屬層的Mn離子會極易遷移到原本鋰層中的Li空位內,形成所謂的“類尖晶石”結構,這些變化造成了目前富鋰錳基材料的一大難題:電壓衰減。近來,研究者們嘗試采用諸多不同方法來穩定結構,抑制氧的流失從而緩解電壓的衰減:如采用材料顆粒表面的包覆、引入氧空位、材料內部其他元素的摻雜等,這些方法都在一定程度上緩解了電壓衰減,但很難在根源上解決結構的問題,未來改善之路還有待進一步探索。
結語
近些年來,越來越多的前沿科學工作者們嘗試探索更為新穎的結構或者體系來取代目前這些傳統的正極材料,如引入高軌道元素Nb、Ru、Ir等來構筑新結構;也有Ceder等人提出的無序巖鹽結構。這些可能都是正極材料未來的發展方向,正極材料之于鋰離子動力電池的發展,未來還需有更為長遠的道路要走。
本文為我公司原創,歡迎轉載,轉載請標明出處,違者必究!
請完善以下信息,我們的顧問會在1個工作日內與您聯系,為您安排產品定制服務
評論